|
バイオAIスタートアップのCraif株式会社(所在地:東京都新宿区、代表取締役CEO:小野瀬 隆一、以下Craif)は、東京慈恵会医科大学 総合医科学研究センター 次世代創薬研究部 部長の藤田 雄准教授、市立東大阪医療センター 呼吸器外科 部長の野尻 崇医師らとの共同研究により、尿中に含まれるマイクロRNAをAI(人工知能)で解析することで、採血不要・通院不要の尿検査により肺がんを高精度に早期発見できること、手術前の尿から術後の再発リスクを予測できること、さらに術後の尿中マイクロRNA変動によって再発をモニタリングできる応用可能性を示しました。本研究成果は、2026年4月18日に学術雑誌「npj Precision Oncology」に掲載されました。 |
|
|
|
|
|
|
|
|
|
|
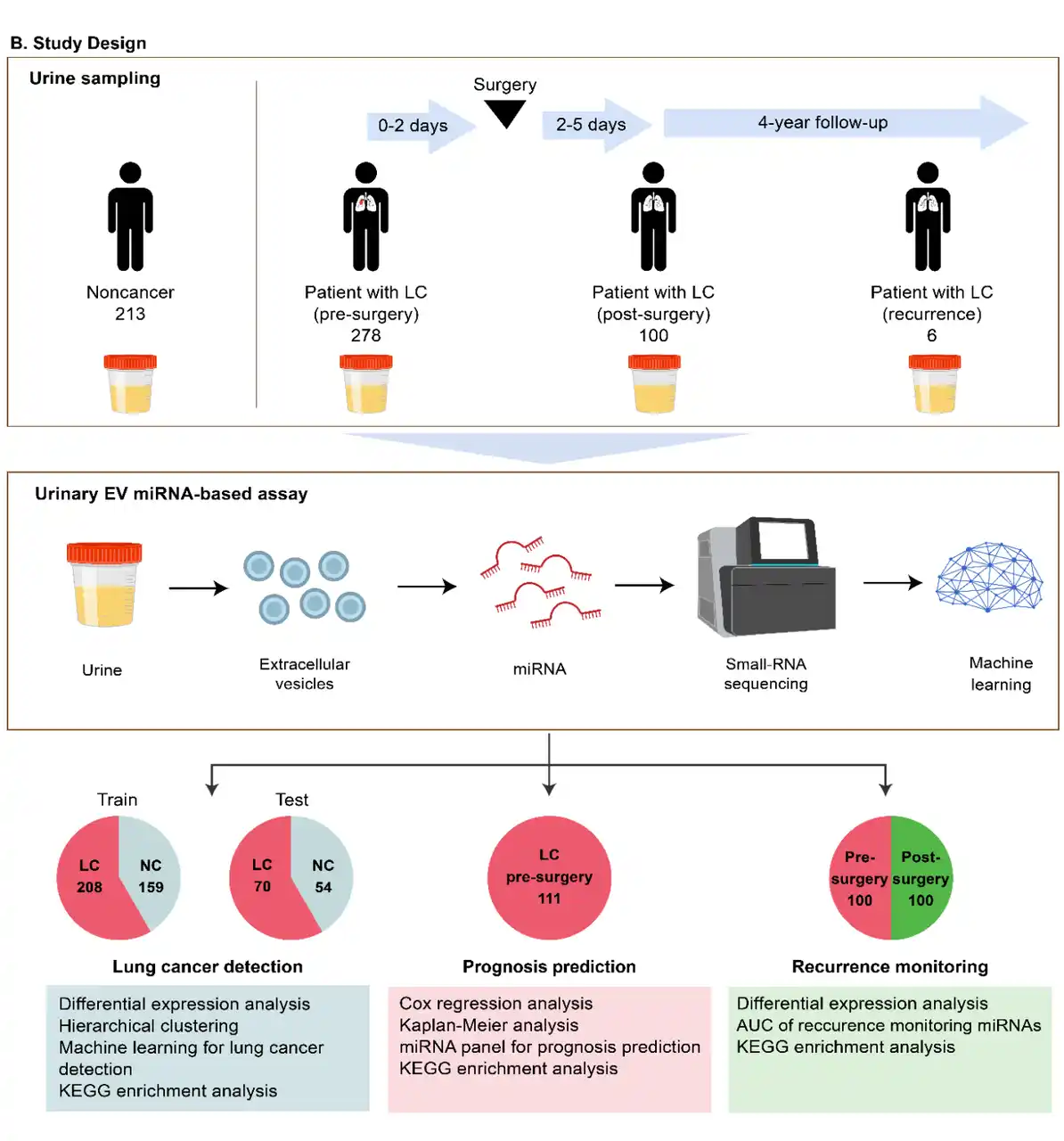
(図1)本研究の概要 |
|
|
|
|
■ 発表のポイント |
|
|
|
1. |
|
早期発見が難しい肺がん:肺がんは世界で最も死亡者数が多いがんです。早期には自覚症状が乏しく、多くの患者が進行してから診断されることが課題です。 |
|
|
2. |
|
多施設共同研究を実施:肺がん患者278名(うち早期ステージが約半数)と非がん者213名から採取した尿サンプルを解析しました。 |
|
|
3. |
|
尿中マイクロRNA検査で早期肺がんを高精度に検出:尿中細胞外小胞由来のマイクロRNAを濃縮・解析し、機械学習モデルを構築することで、早期肺がんを高い精度で検出しました(テストセット:AUC0.941、早期ステージ感度88.2%、特異度87.0%)。 |
|
|
4. |
|
手術前後の尿中マイクロRNA変動で再発モニタリングの可能性:手術により発現が低下し、再発時に再上昇する12種類のマイクロRNAを同定しました。 |
|
|
5. |
|
3種マイクロRNAパネルで術後の再発リスクを層別化:hsa-miR-181a-5p、hsa-miR-185-5p、hsa-miR-934の3種パネルにより、高リスク群と低リスク群で無再発生存期間に大きな差が見られました(HR=8.3)。 |
|
|
6. |
|
単一の尿中マイクロRNAアッセイプラットフォームで肺がん診療の複数フェーズに対応:本プラットフォームは、早期発見・予後予測・再発モニタリングという肺がん管理の異なるフェーズを、1つの検査基盤で包括的にカバーできる可能性を示しました。 |
|
|
7. |
|
自宅採尿が可能な非侵襲的検査:尿を用いるため採血不要で、自宅でのサンプル採取も可能です。広範な集団スクリーニングや、医療機関へのアクセスが限られた地域での活用が期待されます。 |
|
|
|
|
|
|
|
■ 本研究の概要 |
|
|
|
肺がんは男性では最も罹患数が多く、女性でも2番目に多いがんであり、世界で最も死亡者数が多いがんです。早期には自覚症状がほとんどなく、発見されたときには既に手術で取り除くことが難しいステージに進行していることが多いため、早期発見が治療の鍵となります。また、早期ステージで手術を受けた患者であっても、術後に再発するリスクが残ります。現行の血液腫瘍マーカー(CEAやCYFRA21-1など)は早期肺がんに対する感度が低く、より精度の高い非侵襲的な検査法の開発が求められています。 |
|
|
|
そこで研究チームは、がん細胞の活動に深く関わる細胞外小胞とマイクロRNAに着目しました。細胞は細胞外小胞に含まれるマイクロRNAを介して体内の離れた細胞へ情報を伝達しており、がん細胞もこの仕組みを積極的に利用していると考えられています。尿中の細胞外小胞を濃縮することで、尿から大量のマイクロRNAを効率よく抽出・解析できることに着目し、非侵襲的な肺がん検査の開発に取り組みました。 |
|
|
|
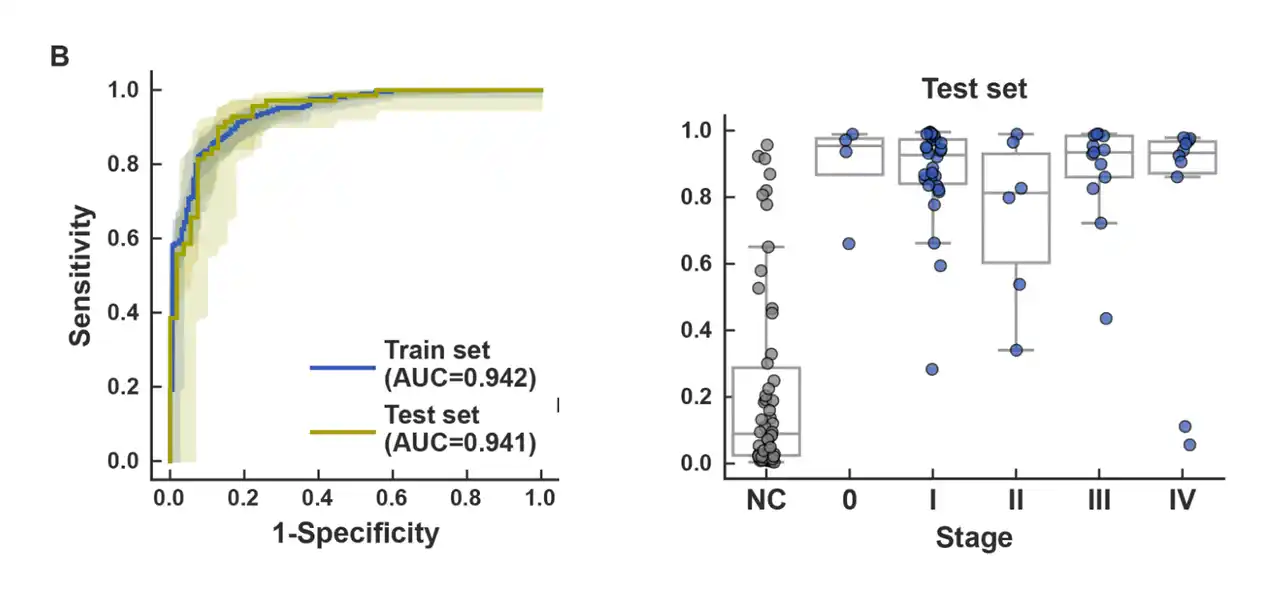
本研究では、4施設(慈恵医科大学病院、東大阪市立医療センター、北斗病院、大宮シティクリニック)から肺がん患者278名(うち早期ステージ〔ステージ0/I〕が約半数)と非がん者213名の尿サンプルを収集し、Small-RNAシーケンシングと機械学習を用いて解析しました。構築された肺がん検出モデルは、トレーニングセットでAUC 0.942、独立したテストセットでもAUC 0.941と高い性能を示しました。特に早期ステージの肺がんに対して、テストセットで感度88.2%、特異度87.0%を達成しました(図2)。また、予測スコアは年齢・性別・BMI・喫煙歴といった背景因子の影響を受けないことも確認されました。 |
|
|
|
|
|
|
(図2)肺がん検出モデルのROC曲線(左)およびテストセットにおけるステージ別予測スコア分布(右) |
|
|
|
|
|
|
再発モニタリングへの応用として、手術前後の尿サンプルを比較解析したところ、肺がん群で高発現し、術後に低下する12種類のマイクロRNAを同定しました。これらのマイクロRNAは再発時に再び上昇する傾向を示しており、腫瘍の存在を反映するバイオマーカーとしての可能性が示唆されました。 |
|
|
|
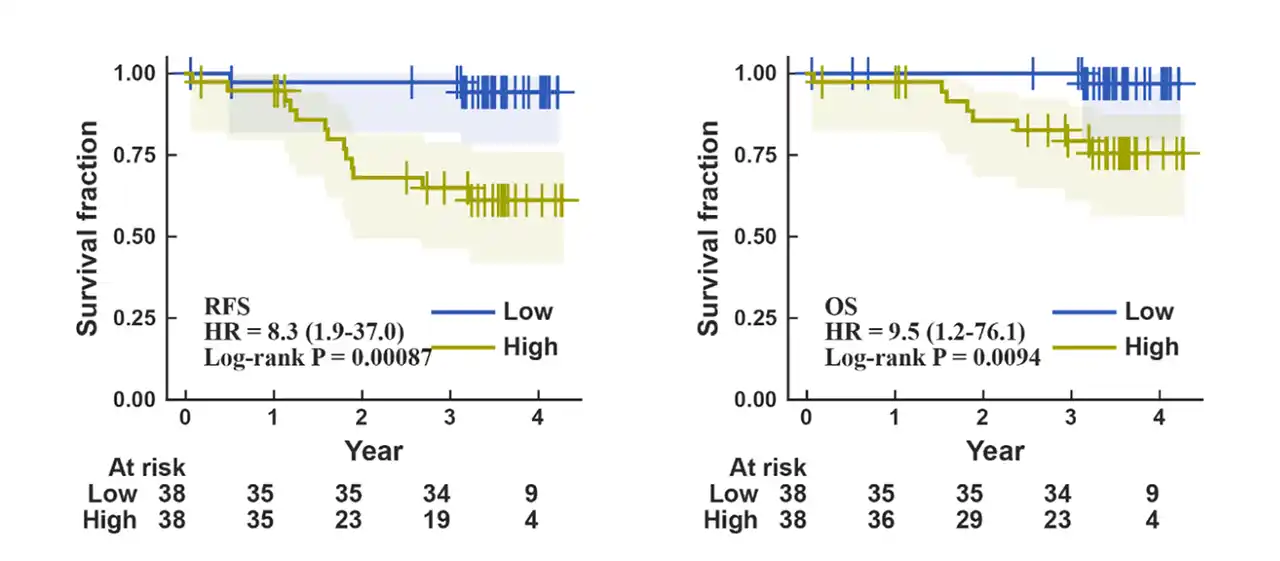
さらに、術後の再発リスク予測を目的として、ステージI/IIの肺がん患者76名を対象にCox回帰解析を実施しました。11種類のマイクロRNAが無再発生存期間と有意に関連しており、そのなかからhsa-miR-181a-5p、hsa-miR-185-5p、hsa-miR-934の3種パネルを構築しました。このパネルにより患者を高リスク群と低リスク群に層別化したところ、無再発生存期間(HR=8.3、p=0.00087)および全生存期間(HR=9.5、p=0.0094)のいずれにおいても、両群間に統計的に有意な差が認められました(図3)。 |
|
|
|
|
|
|
(図3)3種マイクロRNAパネルによる無再発生存期間(左)・全生存期間(中)のカプランマイヤー曲線 |
|
|
|
|
|
|
本研究で示された尿中マイクロRNAアッセイプラットフォームは、1.早期発見、2.予後予測、3.再発モニタリングという肺がん診療の複数フェーズを、単一の検査基盤で包括的にカバーできる可能性を示しています。尿を用いた検査であるため採血不要で患者負担が少なく、自宅でのサンプル採取も可能です。これにより、広範な集団スクリーニングや、医療機関へのアクセスが限られた地域における肺がんの早期発見・管理への貢献が期待されます。 |
|
|
|
|
|
|
|
■ 用語説明 |
|
|
|
• |
|
マイクロRNA:細胞内に存在する非常に小さなRNA分子で、遺伝子の働きを調節する役割を持っています。がん細胞ではマイクロRNAの種類や量が変化するため、病気の早期発見や診断の手がかりとなります。 |
|
|
• |
|
細胞外小胞:細胞が分泌する小さな袋状の粒子で、体内の情報伝達に使われます。細胞外小胞にはマイクロRNAなどの物質が含まれており、がんの診断に役立つ重要な情報を運んでいます。 |
|
|
• |
|
リキッドバイオプシー:血液や尿などの体液を用いてがんを検出する検査法の総称です。組織を採取する従来の生検と異なり、患者への負担が少ない非侵襲的な検査として注目されています。 |
|
|
• |
|
機械学習:AI(人工知能)技術の一種で、大量のデータをもとに自らパターンを学習し、予測や分類を行います。本研究では、マイクロRNAのデータを用いて肺がんの有無を高精度に判定するために用いられました。 |
|
|
• |
|
AUC(曲線下面積):診断検査の正確さを示す指標で、0から1までの値をとります。1に近いほど診断性能が高いことを意味し、一般的に0.9以上は非常に優れた性能とされています。 |
|
|
• |
|
感度・特異度:感度とは、疾病のある人のうちで陽性となる割合を示します。特異度とは、疾病のない人のうちで陰性となる割合を示します。 |
|
|
• |
|
無再発生存期間(RFS):治療後に再発することなく生存している期間を指します。がん治療の効果を評価する重要な指標の一つです。 |
|
|
• |
|
全生存期間(OS):治療開始後から死亡までの期間を指します。無再発生存期間とともに、がん治療の効果を評価する重要な指標の一つです。 |
|
|
• |
|
ハザード比(HR):2つのグループ間でイベント(再発や死亡など)の発生リスクを比較する指標です。HR=8.3は、高リスク群が低リスク群と比べて再発リスクが8.3倍高いことを意味します。 |
|
|
|
|
|
|
|
■ 論文情報 |
|
|
|
• |
|
掲載誌:npj Precision Oncology |
|
|
• |
|
タイトル:A Noninvasive Urinary MicroRNA-Based Assay for Early Detection of Lung Cancer and Its Potential Application to Prognosis and Recurrence Monitoring: a case-control study |
|
|
• |
|
著者:Ayu Kiritani, Shohei Mori, Takashi Nojiri, Junko Watanabe, Hiroki Yamaguchi, Yoriko Ando, Yumi Nishiyama, Mika Mizunuma, Yuki Ichikawa, Yasutaka Kato, Jun Araya, Takashi Ohtsuka, Masahiko Higashiyama, Yu Fujita |
|
|
• |
|
所属: |
|
1. Division of Respiratory Diseases, Department of Internal Medicine, The Jikei University School of Medicine, Tokyo, Japan |
|
2. Division of Thoracic Surgery, Department of Surgery, The Jikei University School of Medicine, Tokyo, Japan |
|
3. Division of Thoracic Surgery, Higashiosaka City Medical Center, Osaka, Japan |
|
4. Craif Inc., Nagoya, Japan |
|
5. Institute of Innovation for Future Society, Nagoya University, Nagoya, Japan |
|
6. Tenshin Inc., Tokyo, Japan |
|
7. Center for Cancer Genomics, Keio University School of Medicine, Tokyo, Japan |
|
8. Department of Pathology and Genetics, Laboratory of Cancer Medical Science, Hokuto Hospital, Obihiro, Japan |
|
9. Division of Next-Generation Drug Development, Research Center for Medical Sciences, The Jikei University School of Medicine, Tokyo, Japan |
|
10. Center for Exosome Medical Research, The Jikei University School of Medicine, Tokyo, Japan |
|
|
• |
|
|
|
|
|
|
|
■ 研究費 |
|
|
|
先進的医療機器・システム等開発プロジェクト(国立研究開発法人日本医療研究開発機構(AMED)):課題番号JP24he2302007 |
|
|
|
■ Craifについて |
|
|
|
Craif(クライフ)はがん早期発見に取り組む2018年創業のバイオAIスタートアップです。尿をはじめとする体液から、DNAやマイクロRNAなど多様なバイオマーカーを高精度に検出する独自の解析技術基盤「NANO IP(R)(NANO Intelligence Platform)」とAI技術を融合し、がんの超早期発見・早期治療・早期復帰を可能にする革新的な検査を開発しています。バイオテクノロジーとAIの力を社会に広く届けることで、当社のビジョンである「人々が天寿を全うする社会の実現」を推進します。 |
|
|
|
【会社概要】 |
|
|
|
社名:Craif株式会社(読み:クライフ、英語表記:Craif Inc.) |
|
代表者:代表取締役 小野瀬 隆一 |
|
設立:2018年5月 |
|
資本金:1億円(2025年4月1日現在) |
|
事業:がん領域を中心とした疾患の早期発見や個別化医療の実現に向けた次世代検査の研究・開発 |
|
本社:東京都新宿区新小川町8-30 THE PORTAL iidabashi B1F |
|
URL:https://craif.com/
|
|




