|
順天堂大学大学院医学研究科 器官・細胞生理学の小松雅明
主任教授らの研究グループは、細胞内で不要となったタンパク質を分解する仕組み「オートファジー*¹」において、p62*²というタンパク質が形成する凝集体の性質がリン酸化*³によって変化し、その分解効率が決まることを明らかにしました。細胞内では、変性して機能を失ったタンパク質は最終的に「ユビキチン*⁴」という目印が付加され分解されます。本研究では、変性して機能を失い、ユビキチンが付加されたタンパク質を集めるp62凝集体が、リン酸化によってよりコンパクトな状態へと変化し、分解に適した性質を獲得することを示しました。本成果は、神経変性疾患などに関わるタンパク質品質管理の理解に貢献することが期待されます。本論文はEMBO Journal誌のオンライン版に2026年5月5日付で公開されました。 |
|
|
|
本研究成果のポイント |
|
● p62凝集体におけるリン酸化制御機構(TBK1とPP2A)を明らかにした |
|
● リン酸化により凝集体が「流動的」から「コンパクトな状態」へ変化することを確認 |
|
● 凝集体の“性質”そのものが、不要タンパク質の分解効率を決めることを示した |
|
|
|
|
|
背景 |
|
細胞内では、変性や損傷によって機能を失ったタンパク質が蓄積すると、細胞機能の破綻や疾患の発症につながります。これらのタンパク質には「ユビキチン」と呼ばれる目印が付加され、オートファジーによって分解されます。p62は、こうしたユビキチンが付加されたタンパク質を集めて凝集体(p62ボディ)を形成し、分解へ導く重要な役割を担っています。近年、この凝集体は液体のような性質を持つ構造として理解されてきましたが、どのような状態の凝集体が効率よく分解されるのかは明らかではありませんでした。本研究では、p62のリン酸化に着目し、その役割の解明を目指しました。 |
|
|
|
内容 |
|
本研究では、p62凝集体におけるリン酸化制御とその機能を明らかにするため、培養細胞解析、in
vitro再構成実験、顕微鏡観察および遺伝子改変マウスを用いた解析を組み合わせた統合的解析を行いました。その結果、リン酸化酵素TBK1と脱リン酸化酵素PP2Aが、p62のリン酸化状態を調節していることが明らかとなりました。さらに、p62の特定部位(Ser403)のリン酸化により、凝集体は大きく流動的な状態から、小さくコンパクトで安定な状態へと変化することが分かりました。この変化により、オートファジーに関わる膜構造との相互作用が促進され、凝集体の分解が効率的に進むことが示されました。
また、この現象は培養細胞だけでなくマウス個体においても確認されました。以上の結果から、p62のリン酸化は凝集体の性質を変化させることで、不要タンパク質の分解効率を左右する分子スイッチとして機能することが示されました。 |
|
|
|
今後の展開 |
|
本研究は、タンパク質の分解効率が凝集体の「性質」によって規定される可能性を示したものです。これまでオートファジー研究は分解経路そのものに焦点が当てられてきましたが、本成果は分解対象の物性制御という新たな視点を提供します。今後、この仕組みが神経変性疾患やがんなど、異常タンパク質の蓄積を特徴とする病態においてどのような役割を担うかを解明することで新たな治療戦略の開発につながることが期待されます。 |
|
|
|
|
|
|
|
|
|
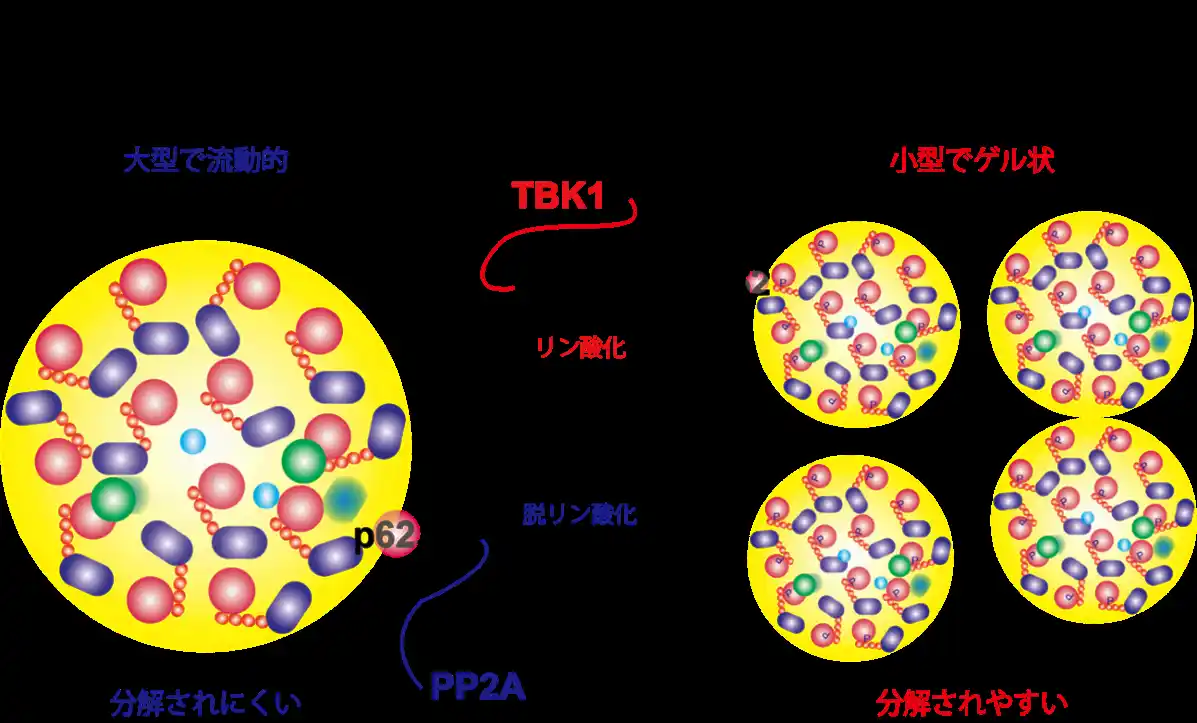
図1:タンパク質の“かたまりの性質”が分解効率を決める |
|
細胞の中では、不要になったり傷ついたタンパク質は「オートファジー」という仕組みによって分解されます。その際、p62というタンパク質がこれらを集めて「かたまり(凝集体)」を作り、分解へと導きます。この図は、そのp62の凝集体の性質が「リン酸化」という化学的な変化によって大きく変わることを示しています。リン酸化が少ない状態では、p62凝集体は「大きくて流動的(液体のよう)」であり、分解されにくい状態にあります。
一方、TBK1という酵素によってp62がリン酸化されると、p62凝集体は「小さくてやや固い(ゲル状)」になり、分解されやすくなります。この変化は、PP2Aという酵素によって元に戻すこともでき、可逆的に変化します。つまり、p62凝集体は単なる「集まり」ではなく、その性質(柔らかさや大きさ)によって分解のされやすさが決まることがわかりました。 |
|
|
|
用語解説 |
|
*1 オートファジー: 細胞内の不要物や異常タンパク質を分解する仕組み。 |
|
*2 p62: ユビキチンが付加されたタンパク質を集めて分解へ導くタンパク質。 |
|
*3 リン酸化: タンパク質の機能や性質を変化させる化学修飾。 |
|
*4 ユビキチン: 分解すべきタンパク質に付加される目印分子 |
|
|
|
研究者のコメント
|
|
本成果は、高い専門性を有する技術職員が筆頭著者として中心的に関与し、緻密な解析を積み重ねたことによって得られたものです。細胞内の品質管理機構の理解を深める成果であり、今後は疾患との関連解明や応用展開を進めていきたいと考えています。 |
|
|
|
|
|
原著論文 |
|
本研究はEMBO Journal誌のオンライン版に2026年5月5日付で公開されました。 |
|
タイトル: Phosphorylation tunes p62 condensates to drive autophagic degradation of ubiquitinated proteins |
|
タイトル(日本語訳): リン酸化によるp62コンデンセートの制御は、ユビキチン化タンパク質のオートファジー分解を駆動する |
|
著者: Satoko Komatsu-Hirota, Keisuke Tabata, Yu-shin Sou, Soichiro Kakuta, Jun-ichi Sakamaki, Hikaru Tsuchiya, Jiachen Li, Hiroyuki Kumeta, Yuji Sakai, Yuko Fujioka, Daisuke Noshiro, Shunsuke F. Shimobayashi, Tomo Kurimura, Takashi Taniguchi, Manabu Abe, Masato Koike, Hideaki Morishita, Nobuo N Noda, Masaaki Komatsu |
|
著者(日本語表記): 小松聡子1)、田端桂介1)、曽高友深2)、角田宗一郎3)、坂巻純一1)、土屋光1)、李佳晨1)、久米田博之4)、境祐二5)、藤岡優子6)、能代大輔6)、下林俊典7)、栗村朋7)、谷口貴志8)、阿部学9)、小池正人2)、森下英晃10)、野田展生6)、小松雅明1) |
|
著者所属: 1)順天堂大学大学院医学研究科器官・細胞生理学講座、2)順天堂大学大学院医学研究科神経機能構造学講座、3)順天堂大学大学院医学研究科研究基盤センター(形態解析イメージング研究室)、4)北海道大学 大学院先端生命科学研究院附属施設次世代物質生命科学研究センター、5)横浜市立大学理学部理学科生命ナノシステム科学研究科物質システム科学専攻、6)北海道大学 遺伝子病制御研究所生命分子機構分野、7)京都大学iPS細胞研究所未来生命科学開拓部門、8)京都大学大学院工学研究科化学工学専攻、9)新潟大学脳研究所生命科学リソース研究センター、10)九州大学大学院医学研究院生体機能学分野 |
|
|
|
DOI: 10.1038/s44318-026-00785-1 |
|
|
|
本研究はJSPS科研費JP23K20044, JP24H00060, JP25H01323, JP24H01901, JP23K27134, JP23K06065, JP25H01419, JP25H00966, JP25H01320, JP25H0132, JP25H00315, P22H04926およびAMED JP22gm1410004h0003, 21gm6410019h0001, JST-CREST JPMJCR20E3,公益財団法人 武田科学振興財団、公益財団法人 上原記念生命科学財団、公益財団法人 小林財団、公益財団法人 三菱財団の支援を受け多施設との共同研究の基に実施されました。 |
|
|
|
なお、本研究にご協力いただいた皆様には深謝いたします。 |
|