| 当社の子会社で医薬品等製造事業を行うアルフレッサ ファーマ株式会社(本社:大阪市、代表取締役社長執行役員:荒木勝利、以下「アルフレッサ ファーマ」)は、本日、群馬工場において新たな医薬品製造棟を稼働いたしましたので、下記のとおりお知らせいたします。 | |||
| 記 | |||
| 1.背景と目的 | |||
| アルフレッサグループは、2032年度までの成長戦略「アルフレッサグループ中長期ビジョン」※1および「25-27 中期経営計画 Vision2032 Stage2 ~総合力で未来を切り拓く~」※2において、医薬品等の導入・開発、製造から物流・販売、市販後調査(PMS※3)・ラストワンマイルまでをグループ一体となって提供するトータルサプライチェーンサービス(TSCS※4)を事業戦略の柱に位置付けております。また、TSCSの機能を活用し、海外の新興バイオ医薬品企業等が日本へ参入する際の障壁を取り除き、スピーディーな市場参入を実現するべく、日本市場への参入を包括的に支援するプラットフォーム「PATH-Solution(商標出願中)」のサービス提供を開始しております※5。 | |||
| アルフレッサ ファーマは、医薬品の製造・販売および診断薬・医療機器・医薬品原材料の製造・輸出入・販売に加え、2005年の薬事法改正により医薬品製造の全面外注化が可能になったことを受け、2009年から医薬品・医薬部外品等の受託製造を本格化しております。同社は、成長領域における取り組みの一つとして受託製造の拡大を掲げ、より効率的で高品質な製造体制の構築を目指し、2024年より新たな医薬品製造棟の建設を進めてまいりました※6。 | |||
| 今回の新棟稼働により、低分子医薬品の生産体制の強化に加え、高薬理活性製剤※7の受託製造や無菌製剤※8の検査・包装・試験受託への本格参入を実現します。これにより、当社グループのTSCSにおける開発から製造までの機能の進化と拡大を図り、多様なモダリティの医薬品を、それらを必要とされている医療機関や患者様に「安心」「安全」「誠実」にお届けできる体制をより強固にしてまいります。 | |||
| ※1 ご参考:2023年5月15日発表 | |||
| 「アルフレッサグループ中長期ビジョン」策定のお知らせ | |||
| https://ssl4.eir-parts.net/doc/2784/tdnet/2281689/00.pdf | |||
| ※2 ご参考:2025年5月15日発表 | |||
| 「25-27 中期経営計画 Vision2032 Stage2 ~総合力で未来を切り拓く~」策定のお知らせ | |||
| https://ssl4.eir-parts.net/doc/2784/ir_material21/256657/00.pdf | |||
| ※3 PMS:(Post Marketing Surveillance)医薬品や医療機器が販売された後に行われる品質、有効性および安全性の確 | |||
| 保を図るための調査 | |||
| ※4 TSCS:アルフレッサグループ全体で保有する様々な機能を有機的に一体活用することで、シームレスなサプライチェ | |||
| ーンを確立し、医薬品等の導入・開発、製造から、物流・販売、市販後調査・ラストワンマイルまでをグループ一体 となって提供することを指しています。 | |||
| ※5 ご参考:2026年1月30日発表 | |||
| 「ドラッグ・ラグ/ロス」の解消へ向けた 海外新興バイオ医薬品企業等の日本参入支援プラットフォーム | |||
| 「PATH-Solution」 サービス提供開始のお知らせ | |||
| https://ssl4.eir-parts.net/doc/2784/ir_material15/272407/00.pdf | |||
| ※6 本新棟の建設は、当社が策定した「ソーシャルボンド・フレームワーク」に基づき、外部評価機関によるセカンド・パ | |||
| ーティ・オピニオンを取得したソーシャルボンドの調達資金の使途の一つであり、社会課題の解決に資する取り組みと | |||
| して位置付けられています。 | |||
| (ご参考:2023年11月7日発表「ソーシャルボンド発行に関するお知らせ」) | |||
| https://ssl4.eir-parts.net/doc/2784/tdnet/2355084/00.pdf | |||
| ※7 高薬理活性製剤:少量で人体に強い薬効を与える成分を含み、取扱いや製造に安全確保のための特別な設備や手順が必 | |||
| 要とされる医薬品 | |||
| ※8 無菌製剤:生育可能な微生物が存在しない状態であることが保証された医薬品。例えば、注射剤として用いられるバイ | |||
| アル製剤やアンプル製剤、シリンジ製剤などが挙げられます。 | |||
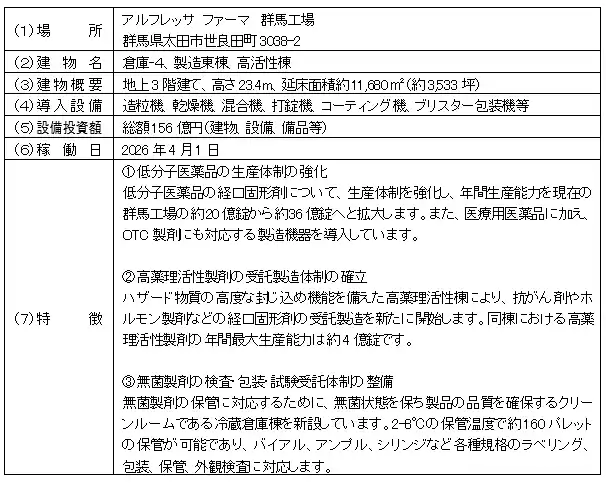
| 2.新たな医薬品製造棟の概要 | |||
|
|||
| 3.今後の見通し | |||
| 群馬工場の新たな医薬品製造棟において、今後、PQ※9およびPV※10を経て、早期の商用生産開始を目指しております。本件による今期業績へ与える影響は軽微であると見込んでおりますが、中長期的には当社グループの企業価値向上に資するものと考えております。 | |||
| 今後、本件に関して開示すべき事項が生じた場合には速やかにお知らせいたします。 | |||
| ※9 PQ:(Performance Qualification)設備が実際の製造条件下で承認された性能を発揮することを確認する適格性評 | |||
| 価 | |||
| ※10 PV:(Process Validation)製造プロセスが一貫して品質基準を満たすことを、科学的・文書的に検証する活動 | |||
【アルフレッサ ホールディングス株式会社】 アルフレッサ ファーマ株式会社群馬工場における新たな医薬品製造棟稼働について
アルフレッサ ホールディングス株式会社 | 2026年4月1日 13:19
📈 本日の注目トレンド(24時間)
- イタンジ、芳根京子さんを起用した新TVCM「覚悟の瞬間」篇、 2026…
- 【渋谷スクランブルスクエア株式会社】 SHIBUYA QWS「Ques…
- 【日本トリム】 日本トリムの農業用電解水素水整水器を活用電解水素水で育…
- 【アイチューザー株式会社】 アイチューザー 奈良県と連携協定を締結
- 【株式会社本田事務所】 アジアビジネスの最前線と未来戦略を探るビジネス…
- 【近鉄不動産株式会社】 駅直結・体感型ショールーム 4月11日(土)オ…
- 【アトム法律事務所】 【4月10日まで受付】アトム法律グループ、交通事…
- 【株式会社エイトノット】 「東京ベイeSGプロジェクト 令和5年度先行…
- 【株式会社チョイスホテルズジャパン】 【再開発で注目の横浜・関内エリア…
- 【株式会社テー・オー・ダブリュー】 TOW、アジア地域最大級の広告祭「…
📊 今週のランキング記事
- 【株式会社STANDAGE】 STANDAGE、ナイジェリア・ラゴスに…
- 音楽を聴くだけでポイントが貯まるリワード型プラットフォーム「SOUND…
- 日テレ・フジ・日経が相次ぎ特集。店舗に客数増を生み出す『トリイク』、国…
- 株式会社NIKUJILLEと株式会社総合近江牛商社が業務提携WAGYU…
- 【株式会社ファミリーマート】 「コンビニエンスウェア」ブランド初!シチ…
- イタンジ、芳根京子さんを起用した新TVCM「覚悟の瞬間」篇、 2026…
- ~「A-GELギフトポイント」&「A-GELギフトカード」~A-GEL…
- 「ほっともっと」手軽に味わう、もちもち食感!ロールタイプのチヂミが新登…
- 【東京書籍株式会社】 アズキの「ア」は赤色の「あ」? 科学で定説を覆…
- 【株式会社 日立情報通信エンジニアリング】 製造業・プラント向け、Io…