|
発表のポイント |
|
◆神経細胞の軸索初節(Axon Initial Segment, AIS)は、神経機能にとり非常に重要です。その形成に必須なタンパク質 TRIM46 が、モータータンパク質 キネシン‐2(KIF3)によって選択的に輸送される分子機構を明らかにしました。 |
◆細胞生物学的、生化学的解析および小角X線散乱構造解析などの多角的解析により、KIF3/KAP3 複合体には複数の構成パターンが存在し、それぞれが異なるカーゴ特異性をもつことを示しました。特に軸索初節(AIS)に特異的に局在するTRIM46 の輸送には、KIF3B/B/KAP3が重要であることを解明しました。
◆キネシン‐2複合体の構成多様性が、神経細胞内での精密な物質輸送制御を可能にしていることを示し、神経回路形成や神経疾患の分子基盤の理解につながる成果です。 |
|
|
|
|
|
|
|
|
|
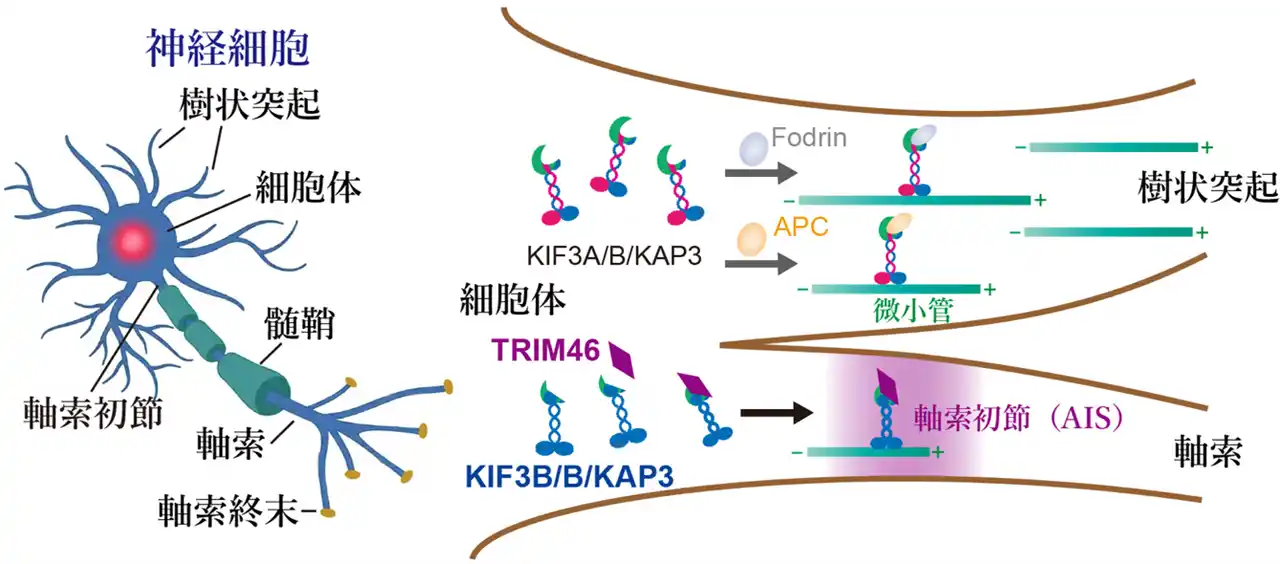
キネシン‐2複合体のサブタイプ分化によるTRIM46の軸索初節(AIS)への選択的輸送モデル |
|
神経細胞において、KIF3A/B/KAP3からなるキネシン‐2複合体が構成の違いによって機能分担し、TRIM46をAISへ特異的に輸送・集積させる模式図。 |
|
|
|
概要 |
|
順天堂大学大学院医学研究科 特任教授/東京大学 名誉教授 廣川 信隆 博士、東京大学大学院医学系研究科 蒋 緒光 特別研究員、群馬大学大学院医学系研究科 一ノ瀬 聡太郎 助教、獨協医科大学先端医科学研究センター 小川 覚之 准教授らによる研究グループは、神経細胞の軸索初節(AIS)(注1)に特異的に集積する構造タンパク質TRIM46(注2)が、モータータンパク質キネシン‐2(KIF3)(注3)により選択的に輸送される分子機構を明らかにしました。 |
|
本研究では、神経細胞を用いた解析から、KIF3Bを含む複合体がTRIM46のAISへの集積に不可欠であることを明らかにしました。これにより、キネシン‐2複合体内での機能分担と輸送特異性の存在が示されました。 |
|
さらに、免疫沈降、プルダウン解析、サイズ排除クロマトグラフィー(SEC)(注4)などの生化学的手法及び小角X線散乱構造解析(注5)を用いて、KIF3A、KIF3B、KAP3からなるキネシン‐2複合体が、組成の異なる複数のサブタイプとして存在することを発見しました。これらのサブタイプは、TRIM46に対する結合性や細胞内分布が異なり、特定のカーゴを選択的に輸送する能力をもつことが示されました。 |
|
|
|
|
|
|
|
|
|
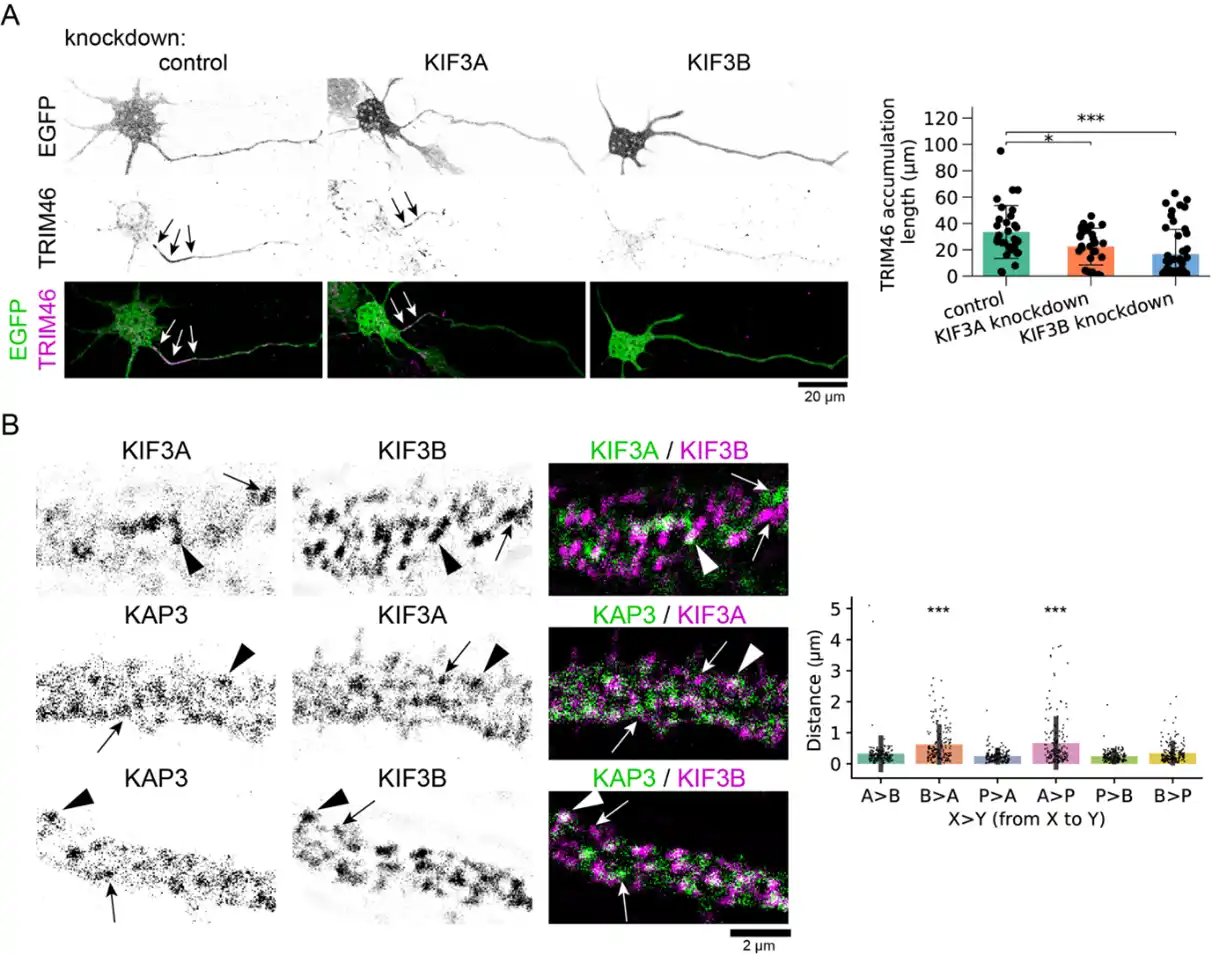
図1:KIF3B依存的なTRIM46の軸索初節集積と神経細胞内分布 |
|
神経細胞におけるTRIM46の軸索初節(AIS)への集積と、キネシン‐2サブユニットによる制御を示す。 |
|
上段(A):TRIM46の免疫染色像。対照条件とKIF3AノックダウンではTRIM46がAISに強く集積するのに対し、KIF3Bノックダウンによりその集積が著しく低下する。右側にAIS長およびTRIM46シグナル強度の定量解析を示す。 |
|
下段(B):キネシン‐2複合体の細胞内分布解析。キネシン‐2の構成要素の局在と密接に相関することを示している。 |
|
これらの結果は、TRIM46のAIS集積がキネシン‐2、とくにKIF3Bを含む複合体に依存していることを示す。 |
|
|
|
発表内容 |
|
神経細胞における物質輸送は、軸索と樹状突起の機能的分化を支える重要な基盤です。特に軸索初節(AIS)は、神経細胞の極性維持や活動電位の発生に必須な領域ですが、そこへ特定のタンパク質を選択的に輸送・集積する分子機構は十分に理解されていませんでした。 |
|
本研究では、神経細胞におけるノックダウン実験により、KIF3Bを含む複合体がAIS形成因子TRIM46の集積に重要であることが示され、キネシン‐2複合体内の構成多様性が、神経細胞における選択的輸送制御の基盤となっていることが示唆されました(図1)。 |
|
さらに、生化学的再構成実験およびSEC解析の結果、KIF3A/B/KAP3 複合体は単一の分子種ではなく、KIF3B/B/KAP3など複数のサブタイプとして存在することが示されました(図2、左)。これらのサブタイプは構造や相互作用様式が異なり、TRIM46との結合性にも差があることが分かりました(図2、右)。特に軸索初節(AIS)に特異的に局在するTRIM46 の輸送には、KIF3B/B/KAP3が重要であることが示されました。 |
本成果は、モータータンパク質による細胞内輸送が「一対一のカーゴ認識」ではなく、複合体の構成変化によって柔軟に制御されていることを示すものであり、神経発生や神経疾患の理解に新たな視点を提供します。 |
|
|
|
|
|
|
|
|
|
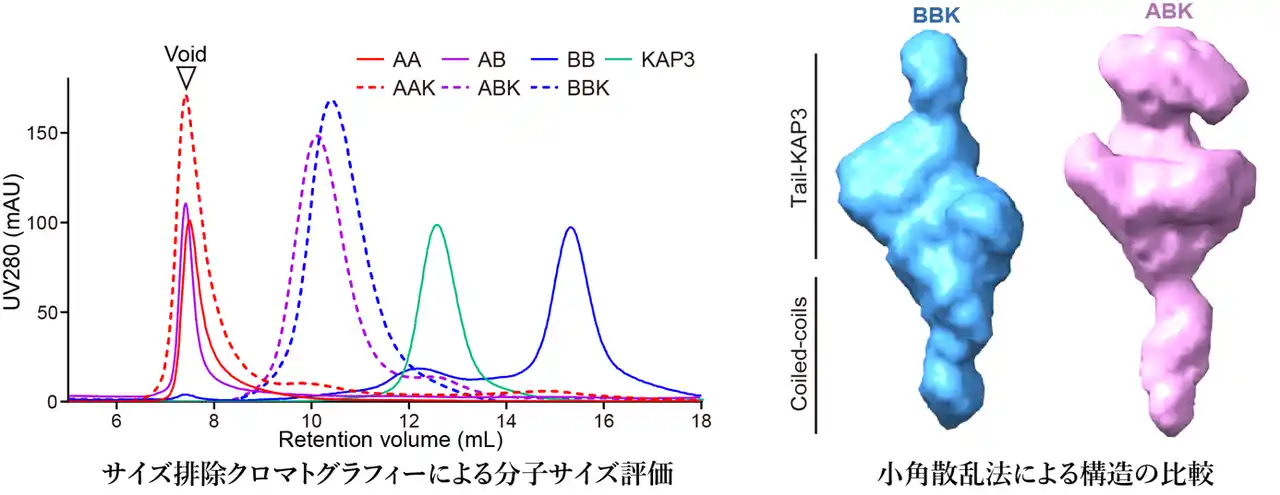
図2:キネシン‐2複合体のサブタイプ形成と構造的特徴 |
|
キネシン‐2複合体が複数のサブタイプとして存在することを示す生化学的および構造的解析。 |
|
左:再構成したKIF3A/B/KAP3複合体の分析用サイズ排除クロマトグラフィー(SEC)。AAK(KIF3A/A/KAP3)、ABK(KIF3A/B/KAP3)、BBK(KIF3B/B/KAP3)など、異なる組成の複合体が明確に分離され、キネシン‐2が単一構造ではなくサブタイプとして存在することを示している。 |
|
右:SAXS解析による複合体構造の比較。異なるサブタイプ間で全体形状やコンフォメーションに差異が認められ、構成の違いが構造的・機能的多様性につながることが示唆される。 |
|
これらの結果は、キネシン‐2複合体のサブタイプ分化が、カーゴ選択性や輸送制御の基盤となっていることを支持する。 |
|
|
|
〇関連情報: |
|
廣川研究室ホームページhttp://cb.m.u-tokyo.ac.jp
|
|
|
|
発表者・研究者等情報 |
|
順天堂大学大学院医学研究科 |
|
廣川 信隆 特任教授(東京大学と兼務) |
|
|
|
東京大学大学院医学系研究科 |
|
蒋 緒光 東京大学特別研究員/日本学術振興会外国人特別研究員 |
|
廣川 信隆 東京大学名誉教授(順天堂大学と兼務) |
|
|
|
群馬大学大学院医学系研究科 |
|
一ノ瀬 聡太郎 助教 |
|
|
|
獨協医科大学先端医科学研究センター |
|
小川 覚之 准教授 |
|
|
|
奈良先端科学技術大学院大学デジタルグリーンイノベーションセンター |
|
米澤 健人 特任助教 |
|
|
|
理化学研究所放射光科学研究センター |
|
清水 伸隆 グループディレクター |
|
|
|
論文情報 |
|
雑誌名: Journal of Cell Biology |
|
題 名: The KIF3B/B/KAP3 tail domain specifically facilitates TRIM46 transport to the axon initial segment |
|
著者名: X. Jiang†, S. Ichinose†, T. Ogawa, K. Yonezawa, N. Shimizu and N. Hirokawa*. †共同筆頭著者 *責任著者 |
|
DOI: 10.1083/jcb.202503138 |
|
|
|
研究助成 |
|
本研究は、科研費「廣川(課題番号:JP25K09633)」、「廣川(課題番号:JP23000013)」、「廣川(課題番号:JP16H06372)」、「一ノ瀬(課題番号:JP24K09994)」、「小川(課題番号:JP24K01519)」、「小川(課題番号:JP20H05499)」、「小川(課題番号:20K07222)」「清水(課題番号:JP19K06516)」、「蒋(課題番号:JP24K18106)」、「蒋(課題番号:JP24KF0141)」、及び日本医療研究開発機構(AMED)創薬等ライフサイエンス研究支援基盤事業創薬等先端技術支援基盤プラットフォーム(BINDS)(課題番号:JP21am0101071)の支援により実施されました。 |
|
|
|
用語解説 |
|
(注1)軸索初節(AIS) |
|
軸索初節は、神経細胞の細胞体と軸索の境界に位置する領域で、活動電位の発生や神経極性の維持に重要な役割を果たします。 |
|
|
|
(注2)TRIM46 |
|
TRIM46(Tripartite motif-containing protein 46)は、神経細胞に特異的に発現するタンパク質で、軸索初節(Axon Initial Segment, AIS)の形成と維持に重要な役割を果たします。TRIM46は微小管に結合し、AISにおいて微小管の配向性を整えることで、神経細胞の極性確立や安定化に寄与することが知られています。TRIM46の機能異常は、神経回路形成の障害や神経機能の破綻につながる可能性が指摘されています。 |
|
|
|
(注3)キネシン‐2 |
|
キネシン-2は、ATPのエネルギーを利用して微小管上を動く分子モータータンパク質の一種です。細胞内でタンパク質や小胞などの荷物(カーゴ)輸送や鞭毛の形成など、多様な細胞機能に関与しています。二つのモータータンパク質と、キネシン関連タンパク質(KAP3)と呼ばれる非モータータンパク質の三者複合体(ヘテロ三量体)として機能するものが多く、記憶・学習などの脳の高次機能、体の左右軸の決定、腫瘍形成の抑制、繊毛成長・機能などの生命現象に関与しています。KIF3A, KIF3B, KIF3C , KAP3 の組み合わせにより複数の複合体が形成され、カーゴ選択性に違いが生じる可能性があります。 |
|
|
|
(注4)サイズ排除クロマトグラフィー(SEC) |
|
サイズ排除クロマトグラフィー(SEC:Size-Exclusion Chromatography)は、溶液中の分子を大きさ(分子サイズ)の違いに基づいて分離する手法です。分子同士が結合して複合体を形成すると、単体の分子とは異なる溶出位置を示すため、タンパク質がどのような複合体として存在しているかを調べることができます。本研究では、キネシン‐2複合体が複数のサブタイプとして存在することを明らかにしました。 |
|
|
|
(注5)小角X線散乱(SAXS) |
|
小角X線散乱(SAXS:Small-Angle X-ray Scattering)は、溶液中に存在するタンパク質やその複合体にX線を照射し、散乱パターンを解析することで、分子全体の形状やサイズ、集合状態を調べる手法です。結晶化を必要とせず、生理的条件に近い状態で解析できることが特徴です。本研究では、キネシン‐2複合体の構成や安定性を評価し、異なるサブタイプの存在を裏付ける構造情報を得ました。 |
|