|
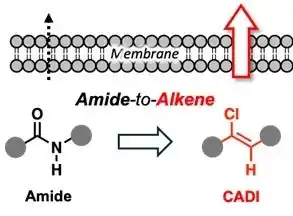
静岡大学大学院総合科学技術研究科 鳴海 哲夫 教授、大吉 崇文 准教授、間瀬 暢之 教授、佐藤 浩平 助教、筑波大学計算科学研究センター 原田 隆平 准教授、北海道大学大学院薬学研究院 渡邉 瑞貴 准教授らによる研究グループは、ペプチド結合 (注1) を、ジペプチドの生物学的等価体(注2)であるクロロアルケンジペプチドイソスター (CADI) (注3) に置換することで、医薬分子として有用な中分子ペプチドの膜透過性を大幅に向上させることに成功しました。 |
|
|
|
|
|
【研究のポイント】 |
|
|
|
■ ペプチドにCADIを導入することで、膜透過性が大幅に向上する分子設計技術を開発 |
|
■ N-メチルアミド、エステル、チオアミドなど既存の主鎖改変と比較し、CADIが最も高い受動的膜透過性を示すことを実証 |
|
■ 鎖状・環状・長鎖ペプチドなど多様な分子系に適用可能であることを確認 |
|
■ 次世代型ペプチド医薬の分子設計指針となる可能性を提示 |
|
|
|
|
中分子ペプチドは、広い相互作用面を利用して標的タンパク質に高い選択性で結合できることから、従来の低分子では難しかったタンパク質間相互作用を標的とする次世代医薬分子として注目されています。しかし、ペプチドは細胞膜を透過しにくく、細胞内の標的に到達できないことが大きな課題となっており、この課題を克服する新しい分子設計技術の開発が強く求められていました。 |
|
|
|
本研究では、ペプチドの主鎖改変に用いられるCADIが水素結合を精密に制御することで疎水性を高め、既知の主鎖改変技術と比較して高い受動的膜透過性を示すことを明らかにしました。さらに、CADIを導入したペプチドでは細胞膜透過性の向上も確認されました。加えて、CADIの適度な疎水性と剛直性により、膜透過性と機能性の両立が可能であることも示されました。 |
|
|
|
本成果は、ペプチドの膜透過性を向上させる新しい分子設計指針を提示するものであり、これまで標的とすることが困難であった細胞内標的を狙う次世代型ペプチド医薬の開発を加速することが期待されます。 |
|
|
|
なお、本研究成果は、2026年2月20日にアメリカ化学会の学術誌 Journal of Medicinal Chemistry に掲載されました。 |
|
|
|
|
|
【研究者コメント】 |
|
|
静岡大学 総合科学技術研究科 教授 鳴海 哲夫
|
|
学生時代から取り組んできたADI研究の新しい可能性を見出しました。中分子ペプチド医薬で真に使える基盤技術として発展させたいと考えています。 |
|
|
|
|
|
|
|
|
|
【研究概要】 |
|
|
|
ペプチド医薬は高い標的結合能と選択性を有することから、次世代医薬品として注目されています。しかし、ペプチドは細胞膜を透過しにくく、細胞内標的に到達できないことが大きな課題となっています。その主な要因は、ペプチド結合が水分子と強固な水素結合ネットワークを形成するため、疎水性の高い細胞膜内部へ移行する際に、大きな脱水和エネルギーを必要とする点にあります。そのため、このエネルギー障壁を低減する新しい分子設計技術の開発が強く求められていました。 |
|
|
|
本研究では、ジペプチドの生物学的等価体であるCADIをペプチドに導入することで、ペプチドの膜透過性を大幅に向上させることに成功しました。計算科学的解析の結果、CADIは水分子との水素結合ネットワーク形成が大きく抑制されることが示されました。 |
|
|
|
また、N-メチルアミドやエステル、チオアミドといった他の生物学的等価体と比較した結果、CADIが最も高い受動的膜透過性 (注4) を示すことを実証しました。さらに、鎖状ペプチドや環状ペプチド、長鎖ペプチドなど多様な分子系においても、一貫してCADIが天然型を上回る細胞膜透過性を示しました。膜透過機構解析の結果、CADIは主にエンドサイトーシス (注5) を介して細胞内に取り込まれていることも見出しました。 |
|
|
|
本研究は、CADIが既存の主鎖改変技術を上回る膜透過性を示すことを体系的に明らかにした初めての研究です。CADIが提示する新しい分子設計指針は、これまで標的とすることが困難であった細胞内標的を狙う次世代型ペプチド医薬の開発を加速するものと期待されます。 |
|
|
|
|
|
【研究背景】 |
|
|
|
中分子ペプチドは、高い標的結合能と選択性を有することから次世代医薬品として期待されていますが、細胞膜透過性が低く、細胞内の標的分子へ到達しづらいことが大きな課題として挙げられます。その主な要因は、ペプチドの主鎖骨格であるペプチド結合にあります。ペプチド結合は、水分子と強固な水素結合ネットワークを形成するため、疎水性の高い細胞膜内部へ移行する際に非常に大きな「脱水和エネルギー」を必要とします。現在、このエネルギー障壁を低減し、膜透過性を向上させる新しい分子設計技術の開発が求められています。 |
|
|
|
|
|
【研究の成果】 |
|
|
|
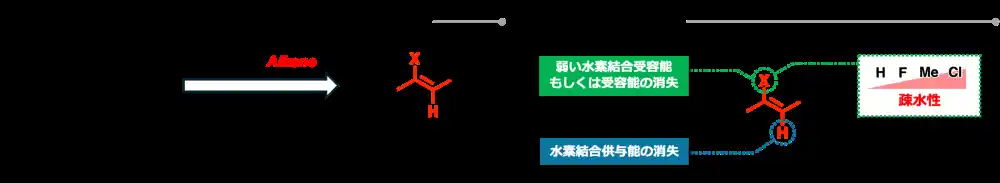
アルケンジペプチドイソスター (ADI) は、ペプチド結合を結合長と結合角がよく似た炭素-炭素二重結合に置換した構造的に類似したバイオイソスターです。これまでの研究から、ペプチドにADIを導入すると、酵素による分解を受けにくくなるだけでなく、ペプチドの形(立体構造)を整えることが可能であることが報告されてきました。本研究では、これまで十分に調べられてこなかったADIの「水素結合の性質」に着目し、それが膜透過性にどのような影響を与えるのかを検証しました (図1)。 |
|
|
|
|
|
|
図1. (A) ADIの特徴と (B) 水素結合能 |
|
|
|
|
|
|
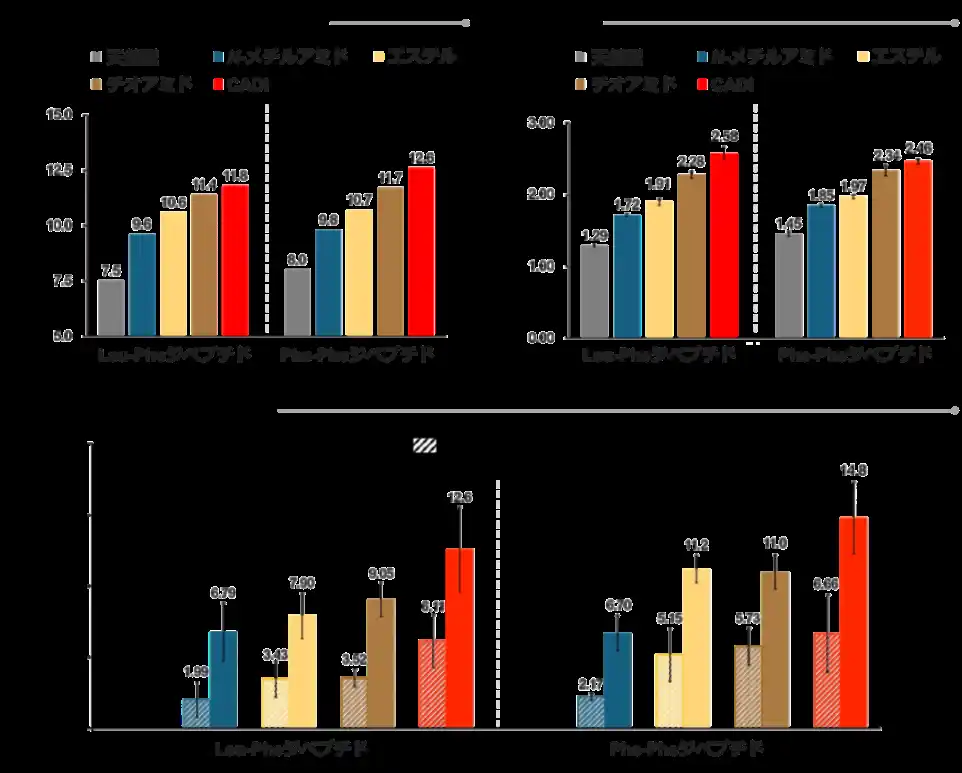
まず、アミノ酸2残基のジペプチドモデルを用いて、これまでにペプチドの膜透過性を向上させる骨格として活用されてきたN-メチルアミド、エステル、チオアミドとCADIの物性を比較しました。具体的には、高速液体クロマトグラフィー (HPLC) によるC18カラムにおける保持時間測定、LogD7.4値の算出および人工膜透過性評価 (PAMPA) (注6) を行いました (図2)。その結果、CADI型は最も高い疎水性を示し、いずれのジペプチドにおいても最も高い受動的膜透過性を示しました。さらに分子動力学計算の結果、CADI骨格周囲では水素結合ネットワークが顕著に弱まっており、この高い疎水性が「脱水和」を促進することで膜透過のエネルギー障壁を下げていることが示唆されました。 |
|
|
|
|
|
|
図2. 各等価体を導入したジペプチドの (A) HPLC保持時間 (B) LogD7.4値 (C) PAMPAによる受動的膜透過性 |
|
|
|
|
|
|
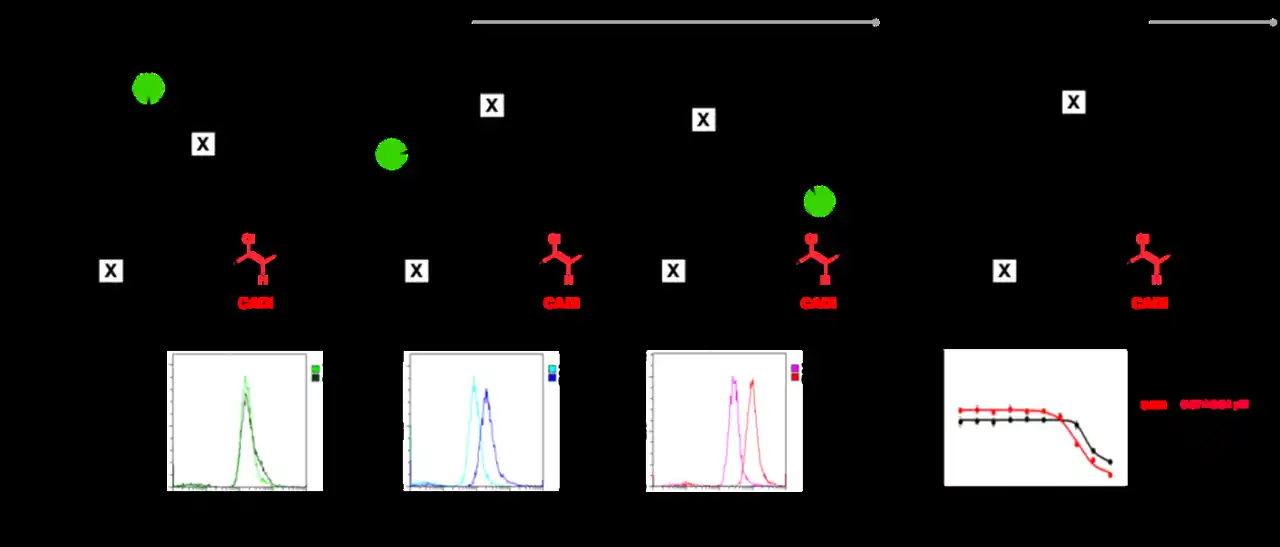
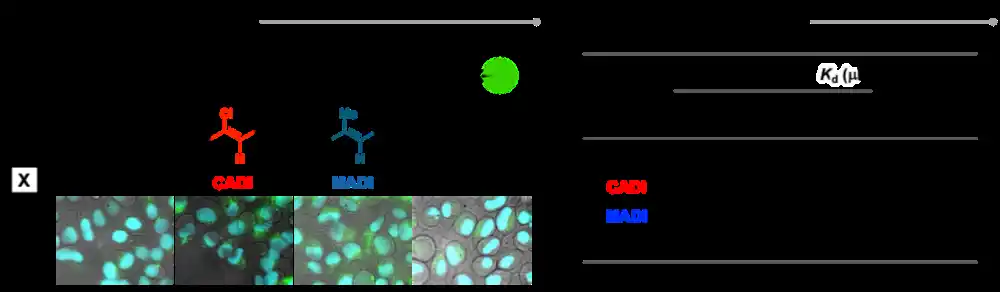
次に、CADIを鎖状ペプチドおよび環状ペプチドに応用し、FACS解析 (注7) により細胞膜透過性を評価しました。その結果、天然型と比較して約2~4倍の細胞膜透過性の向上が認められました (図3)。さらに、細胞質への確実な移行を評価するNanoClickアッセイ (注8) においても、CADI型は透過性が約3倍高いことが確認されました。また、低温条件下およびエンドサイトーシス阻害剤存在下での評価を行ったところ、膜透過性が顕著に低下したことから、CADI型はエンドサイトーシスを介して細胞質に取り込まれていることが示されました。 |
|
|
|
|
|
|
図3. (A) FACS解析を用いた鎖状・環状ペプチドの細胞膜透過性評価 (B) NanoClickアッセイによる環状ペプチドの細胞膜透過性評価 |
|
|
|
|
|
|
最後に、21残基からなるアルギニン-グリシン-グリシン (RGG) ペプチドへと応用し、膜透過性の向上と核酸 (グアニン四重鎖; G4) への結合能の維持が両立できるかを検証しました (図4)。CADIおよびメチルアルケンジペプチドイソスター (MADI) を導入することで、細胞膜透過性を大幅に向上させながら、天然型と同等のG4結合親和性を維持し、さらにG4選択性を向上させることに成功しました。一方で、疎水性は高いものの、構造的に柔軟なアルカン型ではG4結合親和性および選択性が著しく低下しました。この結果から、ADIの「適度な疎水性」と「構造の剛直性」が、膜透過性と機能性を同時に両立させる鍵であることが示されました。 |
|
|
|
|
|
|
図4. RGGペプチドの (A) 細胞膜透過性評価および (B) G4結合親和性・選択性 |
|
|
|
|
|
|
|
|
【今後の展望と波及効果】 |
|
|
|
今回の研究では、CADIがペプチドの膜透過性および細胞内取り込みの双方を向上させる有用な主鎖改変であることが初めて明確に示されました。本研究成果は、ペプチド主鎖の水素結合能を精密に制御することで膜透過性を向上させる新たな分子設計指針を提示するものであり、これにより、細胞内の疾患標的を狙った次世代型ペプチド医薬の開発に貢献することが期待されます。 |
|
|
|
|
|
【論文情報】 |
|
|
|
論文タイトル: |
|
Amide-to-Chloroalkene Substitution for Peptide Backbone Modification to Enhance Membrane Permeability |
|
|
|
著者名: |
|
Sayuri Takeo, Mio Takeda, Chihiro Iio, Ai Sakakibara, Showmitra Saha, Natsuki Shibata, Yuki Yamazaki, Takahiro Fujii, Ryuhei Harada, Kohei Sato, Nobuyuki Mase, Mizuki Watanabe, Takanori Oyoshi* and Tetsuo Narumi* |
|
|
|
掲載誌: |
|
Journal of Medicinal Chemistry |
|
|
|
掲載日: |
|
2026年2月20日 |
|
|
|
DOI: 10.1021/acs.jmedchem.5c02090
|
|
|
|
|
|
【研究助成】 |
|
|
|
本研究は、日本学術振興会 科学研究費助成事業 (JP20H03363, JP23H02601, JP24K08599, JP22K05349)、国立研究開発法人科学技術振興機構 (JST) 次世代研究者挑戦的研究プログラム (SPRING, JPMJFS2119, JPMJSP2167)、ならびに内藤記念科学振興財団および武田科学振興財団の支援を受けて実施されました。また、本研究の一部試薬の提供について、Promega Academic Access Programに感謝いたします。 |
|
|
|
|
|
【用語説明】 |
|
|
|
(注1) ペプチド結合 |
|
アミノ酸のカルボキシ基 (-COOH) とアミノ基 (-NH2) が脱水縮合によって形成された結合。 |
|
|
|
(注2) 生物学的等価体 |
|
分子の物理化学的性質や生物活性を保ちながら、特定の官能基や結合を別の構造へ置き換える分子設計概念。 |
|
|
|
(注3) クロロアルケンジペプチドイソスター(CADI) |
|
ペプチド結合の構造を模倣するアルケンジペプチドイソスターの一種であり、ペプチド結合のカルボニル酸素が塩素原子に置き換えられた構造をもつ分子。 |
|
|
|
(注4) 受動的膜透過性 |
|
分子が細胞のエネルギー消費を伴わず、濃度勾配に従って受動的に移動する性質。 |
|
|
|
(注5) エンドサイトーシス |
|
細胞がエネルギーを消費して細胞外の物質を膜で包み込むようにして細胞内に取り込む能動的な輸送機構。 |
|
|
|
(注6) 人工膜透過性評価 (PAMPA) |
|
人工膜を用いて化合物の受動的な膜透過性を簡便かつ迅速に評価する手法。 |
|
|
|
(注7) FACS解析 |
|
フローサイトメトリー解析。流動する個々の細胞にレーザー光を照射し、散乱光や蛍光を検出することで、細胞内への物質の取り込み量等を統計的・定量的に解析する技術。 |
|
|
|
(注8) NanoClickアッセイ |
|
化合物が細胞内 (特に細胞質) に実際に取り込まれているかどうかを、特定の標的分子に依存せず定量的に評価できる解析手法。 |
|