|
【研究の要旨とポイント 】 |
|
|
|
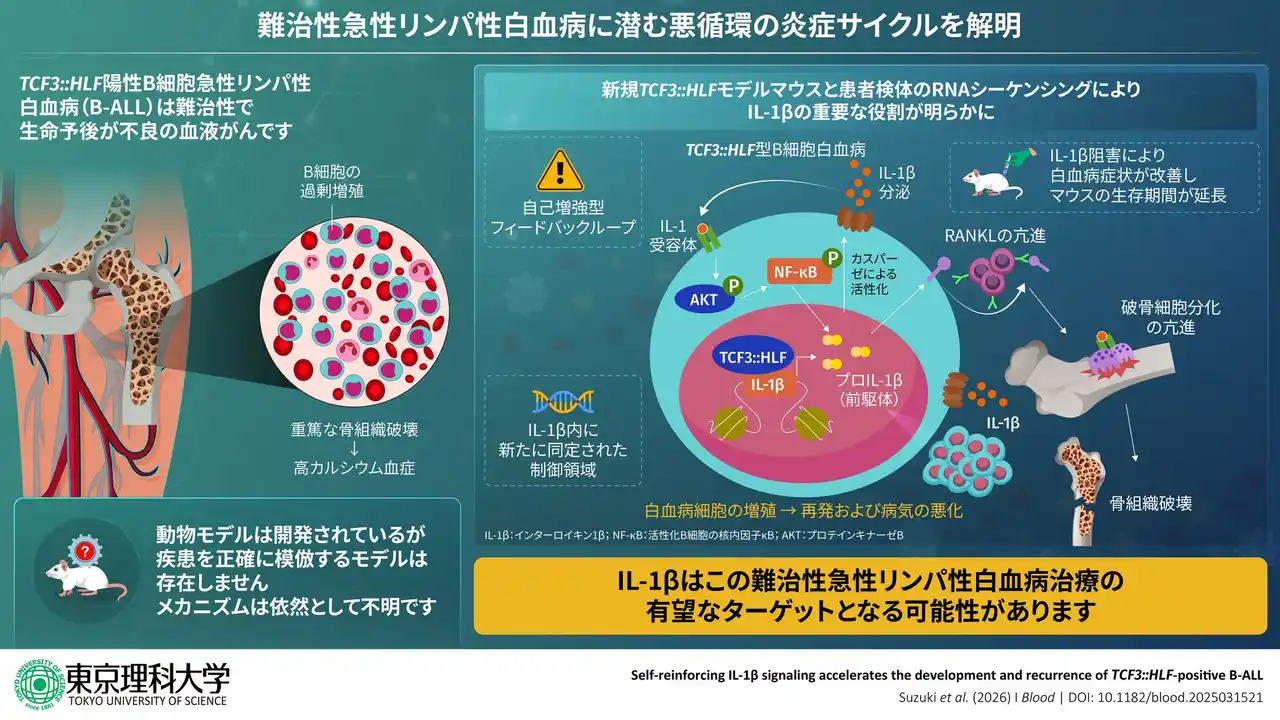
難治性の急性リンパ性白血病においては、なぜ病気が急速に進行し、骨が壊れる深刻な合併症が引き起こされるのかはわかっていませんでした。 |
|
|
|
本研究では、白血病細胞が炎症性サイトカインの一種であるIL-1βを自ら作り出して白血病細胞自身を増殖させるとともに、破骨細胞への分化を促す因子の誘導を介して骨の破壊を促進することを見出しました。 |
|
|
|
今回の成果は、これまで治療が難しかった急性リンパ性白血病の新しい治療法の開発につながる可能性があります。 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
【研究の概要】 |
|
東京理科大学 生命医科学研究所の伊川 友活教授、同大学大学院 生命科学研究科の鈴木 藍彩氏(博士課程3年)、山梨大学大学院 総合研究部 医学域臨床医学系(小児科学)の犬飼 岳史教授らの研究グループは、難治性の急性リンパ性白血病(ALL)において、病気の進行と骨破壊という重篤な合併症が同時に引き起こされる新たな分子メカニズムを発見しました。 |
|
|
|
急性リンパ性白血病の中には、B細胞急性リンパ性白血病(B-ALL)など、治療に抵抗性を示すタイプがあり、治療法の開発が待たれています。B-ALLは、発症後に病気が急速に進行するとともに、骨がもろくなって壊れてしまう深刻な合併症を伴います。しかしながら、病気の悪化と骨破壊がなぜ急激かつ同時に起こるのか、その仕組みはこれまで十分に分かっていませんでした。 |
|
|
|
B-ALLの病態解明が進まない主な原因の一つは、B-ALLの症状や病態を模倣したモデルマウスが未だ存在しないことでした。そこで本研究では、伊川教授らがこれまでに開発した独自技術を用いて難治性ALLの一種である17;19転座型(TCF3::HLF型)B-ALLモデルマウスを作製し、そのマウスを用いて本疾患の背景にあるメカニズムについて調べました。その結果、白血病細胞(*1)が炎症性サイトカインの一種である IL-1β(*2) を自ら作り出し、白血病細胞の増殖を促すとともに、破骨細胞への分化を促すRANKL(*3)の誘導を介して骨の破壊を促進することを明らかにしました。これは、白血病の悪化と骨破壊が同時に進行するという、新たな分子メカニズムの存在を示唆しています。 |
|
|
|
今回の成果は基礎研究として重要なだけではなく、これまで治療が困難であったB-ALLに対して、病気の進行と骨破壊の両方を抑える新しい治療法の開発につながる極めて重要な発見です。 |
|
|
|
本研究成果は、2026年3月3日に国際学術誌「Blood」にオンライン掲載されました。 |
|
|
|
【研究の背景】 |
|
ALLは、血液のがんの一種で、特に小児や若年層に多く発症することが知られています。近年の治療法の進歩により、多くのALLサブタイプ(*4)で治癒が期待できるようになってきましたが、中には特定のB-ALLなど、治療が効きにくく、再発を繰り返す難治性のサブタイプが存在します。こうした難治性ALLでは、病気が急速に進行し、生命予後が不良であることが大きな課題となっています。 |
|
|
|
また、難治性ALLでは、骨がもろくなったり壊れたりする骨破壊を伴う重い合併症がみられることがあります。骨破壊は、強い痛みや運動障害を引き起こすだけでなく、造血機能の低下や治療の継続を困難にするなど、患者の生活の質や治療成績に深刻な影響を与えます。しかしながらこれまで、白血病の悪化と骨破壊がなぜ同時に起こるのか、その分子レベルでの仕組みは十分に解明されていませんでした。 |
|
|
|
そこで本研究では、特定の遺伝子異常によって生じる難治性B-ALL(TCF3::HLF陽性B-ALL)に着目しました。TCF3::HLF陽性B-ALL患者は、高度の骨破壊と高カルシウム血症を呈することから、その発症の分子的なメカニズムが明らかになれば、難治性ALLにおいて病気の進行と骨破壊を同時に引き起こされる共通の原因の解明につながると考え、モデルマウスの作製に着手しました。 |
|
|
|
【研究結果の詳細】 |
|
本研究グループはまず、伊川教授らが2015年に開発した多能性血液前駆細胞であるiLS細胞(人工白血球幹細胞、*5)を用いて、TCF3::HLF陽性B-ALLの特徴を再現するモデルマウスを作製しました。作製したモデルマウスでは、病気の進行(白血病細胞の浸潤、脾腫‧リンパ節腫大)と、骨破壊(破骨細胞の大幅な増加と骨芽細胞の減少)の両方が確認されました。 |
|
|
|
このモデルマウスを用いて、白血病の進行過程や、骨破壊を伴う重い合併症がどのように引き起こされるのかについて解析しました。 |
|
|
|
骨の形態解析では、TCF3::HLF型B-ALL細胞では、IL-1βなどの炎症性サイトカインの発現が顕著に亢進していることがわかりました。そこで、IL-1β遺伝子あるいはその受容体である IL1R1遺伝子を欠失させると、白血病細胞の増殖が抑制されました。これは、一般的には炎症や免疫反応を調節する役割を持つことで知られるIL-1βが、TCF3::HLF陽性B-ALLではIL-1βが細胞自身に作用して増殖を促進し、病気の進行を加速させていることを示唆しています。 |
|
|
|
さらに、IL-1βあるいはIL1R1遺伝子を欠失させると、RANKL 発現が低下し、骨破壊の改善が確認されました。つまり、IL-1βは白血病細胞の増殖を促進するだけでなく、破骨細胞にも作用し、その働きを強めることが分かりました。 |
|
|
|
これらの結果より、TCF3::HLF陽性B-ALLにおいては、白血病細胞が産生するIL-1βと白血病細胞自身が発現するRANKLが協調し、破骨細胞分化を亢進させることで、白血病の悪化と同時に骨組織破壊を引き起こすということが示されました。 |
|
|
|
本研究で明らかになった分子メカニズムは、難治性急性リンパ性白血病、特にB-ALLにおいて病気の進行と骨破壊を同時に抑える治療法の開発につながる可能性があります。今後は、本研究で特定した分子を標的とした治療法の有効性や安全性についてさらに検証を進めることで、新しい治療法開発への応用が期待されます。 |
|
|
|
|
|
• |
|
本研究は、日本医療研究開発機構(AMED)、公益財団法人アステラス病態代謝研究会、公益財団法人上原記念生命科学財団、日本血液学会研究助成、公益財団法人高松宮妃癌研究基金、公益財団法人ノバルティス科学振興財団、公益財団法人がん研究振興財団、金沢大学がん進展制御研究所・学外共同研究助成、国立研究開発法人科学技術振興機構(JST) FOREST プログラム、日本免疫学会「きぼう」プロジェクトの助成を受けて実施したものです。 |
|
|
|
|
|
|
|
【用語】 |
|
*1 白血病細胞 |
|
白血病によって生じる異常な血液細胞。正常に分化・成熟するはずの血液細胞ががん化することで際限なく増殖し続けるようになり、正常な血液の働きを妨げる。 |
|
|
|
*2 IL-1β(インターロイキン1β) |
|
体内で炎症や免疫反応を調節するタンパク質である炎症性サイトカインの一種。 |
|
|
|
*3 RANKL(receptor activator of NF-κB ligand) |
|
骨細胞や骨芽細胞の表面に発現している膜貫通タンパク質の1種。破骨細胞の前駆細胞は、その表面に膜貫通タンパク質「RANK」を発現しており、RANKLが結合することで活性化され、破骨細胞に分化する。 |
|
|
|
*4 サブタイプ |
|
病理学的な特徴に基づき疾患をさらに細分化したもの。 |
|
|
|
*5 iLS細胞(多能性血液前駆細胞) |
|
さまざまな血液細胞に分化する性質(多分化能)と自己複製する性質(自己複製能)を併せ持った造血前駆細胞。体外で無限に増やせる特性があることから、がんに対する免疫細胞療法への応用などが期待されている。 |
|
|
|
【論文情報】 |
|
|
|
雑誌名 |
:Blood |
|
論文タイトル |
:Self-reinforcing IL-1b signaling accelerates the development and
recurrence of TCF3::HLF-positive B-ALL |
|
著者 |
:Aisa Suzuki, Tsukasa Shigehiro, Mayumi Hirakawa, Risa Hirano,
Minori Tamai, Koshi Akahane, Kazuo Okamoto, Hiroshi Takayanagi,
Yuya Terashima, Satoshi Ueha, Toshimori Kitami, Masatoshi Takagi,
Dai Keino, Hiroshi Kawaguchi, Keisuke Kato, Moeko Hino,
Akihiko Yoshimura, Takeshi Inukai, Tomokatsu Ikawa |
|
DOI |
:10.1182/blood.2025031521
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|