|
千葉大学大学院薬学研究院の福本 泰典講師および小椋 康光教授と、京都薬科大学生化学分野の幸 龍三郎助教らの研究チームは、「活性化されたDNA損傷応答機構がどのように維持され、どのように終結するのか」という、未解明の仕組みを詳細に検討しました。その結果、DNA損傷応答の中心となるシグナル伝達において、複数のタンパク質複合体がエネルギー的に同等な構造変化を段階的に繰り返すことで、「活性化」「維持」「不活性化」という過程を精密に制御している機構を明らかにしました。この成果は、DNA修復機構の理解を深め、新規抗がん剤の開発につながると期待されます。 |
|
本研究成果は、2026年2月5日に、学術誌Nucleic Acids Researchで公開されました。 |
|
(論文はこちら:10.1093/nar/gkag093) |
|
|
|
■研究の背景 |
|
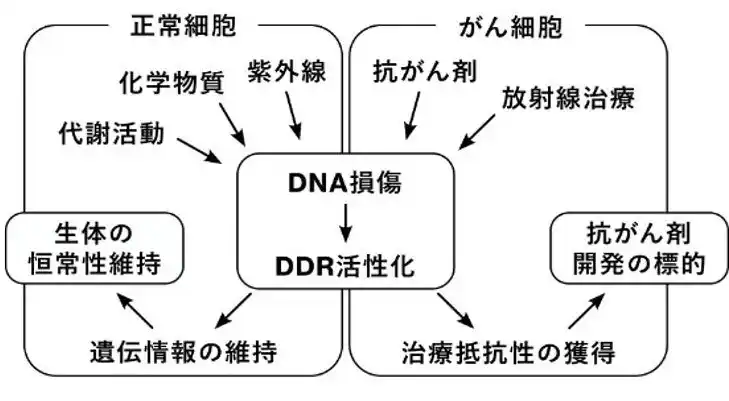
私たちの体を構成する細胞内のDNAは安定していると思われがちですが、紫外線や化学物質、日常的な代謝活動などによって絶えず損傷を受けています。損傷が放置されると、がんや老化、遺伝性疾患などを引き起こします。そこで生物はDNAを修復・保護するDNA損傷応答(DNA Damage Response: DDR)と呼ばれる、仕組みを進化させてきました。一方、がん細胞はDDRを利用することで化学療法や放射線治療に対する耐性を高めるため、DDRは抗がん剤開発の標的ともなります(図1)。 |
|
|
|
|
|
|
図1 DNA損傷応答(DDR)の役割 |
|
|
|
|
代表的なDDRの一つであるATRキナーゼ(注1)依存的DDR(ATR-DDR)についてはDNA損傷を検知して活性化する過程に、研究が集中されてきました。また、DNA損傷部位に多くのタンパク質が集まり、「フォーカス」と呼ばれる塊を作る現象も報告されていました(参考文献)。しかし、なぜ多数のタンパク質が安定に集まれるのか、また、その集積がDDRの活性維持や反応終結にどう関わるのかは、よく分かっていませんでした。 |
|
本研究チームはこれまで、ATR-DDRの中心的な役割を担うタンパク質、Rad17やRad9-Hus1-Rad1(9-1-1)複合体に注目してきました。本研究では、ATR-DDRに関与するタンパク質を個別に解析するのではなく、それらに共通する制御機構があるのではないかという視点から、解析を進めました。 |
|
|
|
|
|
■研究成果のポイント |
|
本研究では、最先端のin silico解析(注2)と生化学的検証を組み合わせ、以下の重要な発見が得られました。 |
|
1.複数のタンパク質に共通する機能的アミノ酸配列(KYxxL+モチーフ)の同定 DNAに傷がつくと、細胞内ではすぐに修理部隊が集まります。その中心になるのが「9-1-1(ナイン・ワン・ワン)」というリング状のタンパク質です(図2)。 |
|
|
|
|
|
|
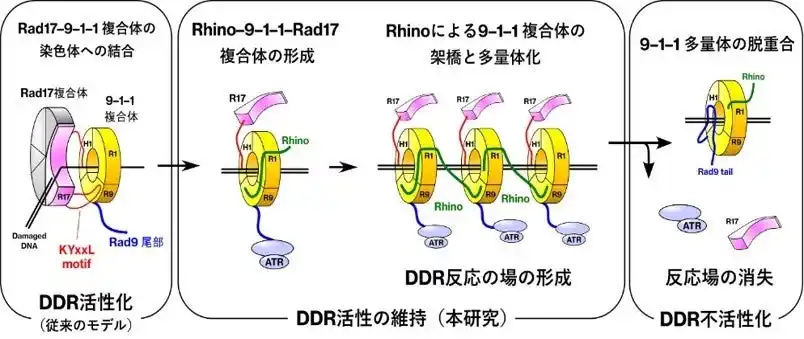
図2 ATR依存的DDRの段階的移行: 活性化したDDRが活性維持段階を経て不活性化段階へと移行するメカニズムを提案。特に、Rad17-9-1-1-Rhino複合体の構造遷移が各段階の移行の基盤となると示唆された。活性維持段階においては、集積したDDR関連タンパク質によってDDR反応の場としてのフォーカスが形成され、DDR不活性化段階においては、DDR関連タンパク質が拡散し、反応の場が消失すると考えられる。 |
|
|
|
|
In silico解析によって、ATR-DDRに関わる複数のタンパク質に共通のアミノ酸配列、KYxxL+モチーフが見出されました。さらにこのKYxxL+モチーフが9-1-1複合体との相互作用に重要であることが示されました。 |
|
|
|
2. ATR-DDRに関わる機能未知タンパク質Rhinoの解析 未解明だったATR-DDRに関わるタンパク質Rhinoが、2つのKYxxL+モチーフを持つことが明らかとなりました。これにより、Rhinoが複数の9-1-1複合体と同時に結合する「架橋因子」として働く可能性が示されました。 |
|
|
|
3. 9-1-1複合体を足場とした複数のタンパク質複合体の形成とその解析 DNA損傷応答の初期段階では、9-1-1複合体の染色体と結合することでDDRが活性化されます。この段階ではRad17-9-1-1複合体が中心的な役割を果たします。本研究によって、Rad17-9-1-1複合体(図2左)に加えて、Rad17-9-1-1-Rhino複合体(図2中央)とRad9 C末尾部-9-1-1複合体(図2右)の三種類の複合体の存在が示唆されました。これらの複合体はそれぞれに、ATR-DDRの活性化、活性維持、反応終結に関与すると考えられます。すなわち、DDRは単一の構造で進行するのではなく、複数の構造状態を経て段階的に制御されている可能性が示されました。
|
|
|
|
4. Rhinoによる9-1-1複合体の架橋と多量体化 上記の解析に基づいて、Rhinoが9-1-1複合体同士を架橋し、DDRの際に9-1-1複合体が多量体化する分子モデルを提唱しました(図2中央)。この9-1-1複合体の多量体化は、従来から観察されていた「フォーカス形成」の分子機構であると考えられます。フォーカス形成は、DDRに関わるタンパク質が集積してDDRのための反応の場を形成していることを意味します。 |
|
|
|
5. エネルギー的に等価なタンパク質複合体構造の変遷 活性化段階、活性維持段階、反応終結段階に関わるタンパク質複合体は、お互いに同程度の安定性を持つことが示され、ATR-DDRがほぼ同じ安定性を持つ複数の状態間を移行する可能性が示されました。これは、エネルギー的に同等なタンパク質複合体の構造遷移によって、ATR-DDRが活性化、活性維持、反応終結へと段階的に移行することを示唆します。 |
|
|
|
■今後の展望 |
|
ATR-DDRはがん細胞の生存に重要であるため、ATRキナーゼなどの阻害剤が抗がん剤として開発されてきました(参考文献)。しかし、骨髄抑制などの副作用が課題となっており、新たなDDRの制御戦略が必要となっています。本研究によって、9-1-1複合体の多量体化がDDRの反応の場としてのフォーカス形成の足場となり、ATR-DDRの活性維持に寄与する可能性が示されました。今後、9-1-1複合体の多量体化を標的としたDDR制御方法の開発などが、新規の抗がん剤の開発戦略などに発展することが期待されます。 |
|
|
|
■用語解説 |
|
注1) ATRキナーゼ: 細胞のDNAに異常が起きたときに働く“見張り役”のたんぱく質。DNAの傷を感知し、細胞分裂を一時停止させて修復をうながす。遺伝情報を守る大切なスイッチのような存在。 |
|
注2)in silico解析: コンピュータを活用してシミュレーションやデータ解析を行い、科学的な問題を解決する手法を指す。この手法は、特に創薬や分子生物学の分野で広く利用されており、従来の実験的手法と比較して、コストや時間を大幅に削減できる。 |
|
|
|
■論文情報 |
|
タイトル: Energetically equivalent structural transitions in the Rad17-Rad9-Hus1-Rad1-Rhino complex underlie the sequential progression from activation through maintenance to inactivation of the ATR-dependent DNA damage response |
|
著者: Yasunori Fukumoto, Ryuzaburo Yuki, Yasumitsu Ogra |
|
雑誌名: Nucleic Acids Research |
|
DOI: 10.1093/nar/gkag093 |
|
|
|
■参考文献 |
|
タイトル: The essential kinase ATR: ensuring faithful duplication of a challenging genome |
|
雑誌名: Nat Rev Mol Cell Biol |
|
DOI: 10.1038/nrm.2017.67 |
|
複数の構造状態を経て段階的に制御されている可能性が示されました。


